2022年4月25日,中美冠科、Merus公司和巴塞罗那科学技术研究院的研究人员合作,在 Nature 子刊 Nature Cancer 发表了题为:《Functional patient-derived organoid screenings identify MCLA-158 as a therapeutic EGFR × LGR5 bispecific antibody with efficacy in epithelial tumors 》的研究论文。
该研究首次使用来自癌症患者的类器官库对500多个双特异性抗体进行筛选,从中发现了名为 MCLA-158 的 EGFR × LGR5 双特性抗体能够有效抑制结直肠癌类器官的生长,并防止转移的发生。
其研究成果为医药公司使用类器官进行药物发现奠定了基础。
什么是类器官?
类器官(Organoids)是以干细胞或器官祖细胞为原料,经过体外培养,能发生细胞分化及谱系定向,即自组装为器官样结构的细胞群,在极大程度上模拟目标组织或器官遗传特征和表观特征。
早在2009 年,Hans Clevers 实验室就使用了单个 LGR5 + 肠干细胞在体外自组织成具有肠隐窝 - 绒毛结构的肠类器官。
这是首个体外自组织的微型器官。也因此,Hans Clevers 被誉为 “国际类器官鼻祖”。
2013年,类器官被 Science 评为年度十大科学技术,Hans Clevers 也因类器官领域的开创性研究获得了2013年科学突破奖(Breakthrough Prize)。
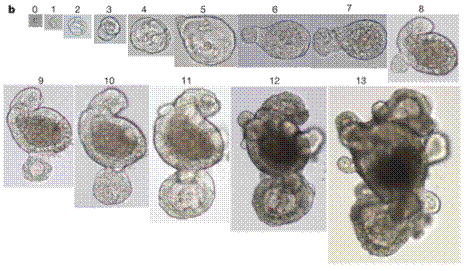
图片来源:Hans Clevers, Nature, 2009
近年来,类器官领域研究成果不断,许多新型类器官和更复杂的类器官也开始涌现。
世界首例由癌症患者为来源的类器官
2021年10月,Merus公司就首次使用来自癌症患者的类器官库,借此对500多个双特异性抗体进行筛选。

他们选中了七名患者,而后做了一系列研究及临床试验,依照数据报告了 MCLA-158 的 EGFR × LGR5 双特性抗体治疗晚期头颈部鳞状细胞癌(HNSCC)的中期临床试验的安全性、耐受性和抗肿瘤活性。
结果显示,7名患者均观察到肿瘤缩小,其中3名得到了部分缓解,1名实现了完全缓解。
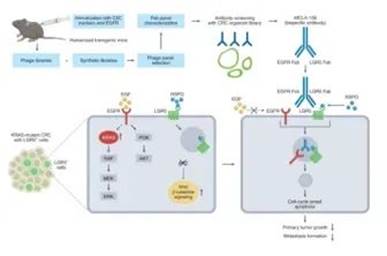
MCLA-158(Petosemtamab):一种双特异性抗体,可识别癌症干细胞表面的两种蛋白——EGFR 和 LGR5,EGFR 促进细胞不受控生长,而 LGR5 则是负责癌症扩散的肿瘤干细胞表面的标志物。
最新发现的双特异性抗体MCLA-158不仅识别出了癌症干细胞表面的两种蛋白——EGFR 和 LGR5(EGFR 促进细胞不受控生长, LGR5 负责癌症扩散的肿瘤干细胞表面的标志物。),还抑制了具有 LGR5 标志物的癌症干细胞中的 EGFR 蛋白,从而阻断引起癌症扩散的肿瘤干细胞的生长和存活。
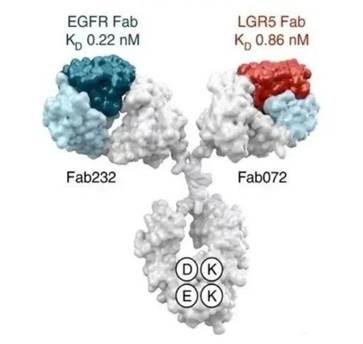
除此之外,他们发现之前的研究显示,MCLA-158 不仅能够抑制头颈部肿瘤、食道肿瘤和胃肿瘤的临床前肿瘤模型的生产,还能抑制结直肠癌类器官的生长和转移。
为了进一步开发和表征该双特异性抗体,HUB Organoids(由类器官的开创者Hans Clevers创建)的研究人员借着这项研究试验建立了一个大型类器官库,里面包括来自结直肠癌患者的类器官、来自结直肠癌转移到肝脏的类器官以及来自正常非癌组织的类器官。
OcellO 公司的科学家对这一类器官库进行了高通量筛选。
在药物开发的早期阶段,使用来自患者肿瘤组织类器官,有助于识别对患者有效的,甚至是对携带特定突变肿瘤有效的治疗性药物。
而使用来自健康组织的类器官,也可以识别对器官产生不良作用的药物,评估药物的有害影响,从而在研究初期撤回毒性作用更大的药物。
在这项研究中,研究团队在结直肠癌患者来源的类器官和健康结肠粘膜来源的类器官进行高通量筛选,从500多种双特异性抗体中发现了 MCLA-158。
MCLA-158 能够特异性触发 LGR5 阳性癌症干细胞中的 EGFR 蛋白降解,而对 LGR5 阳性健康结肠干细胞的毒性很小。
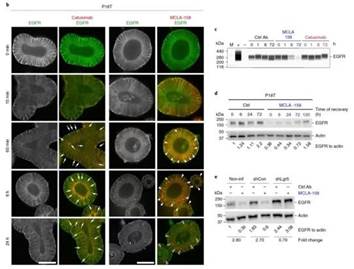
令人振奋的是,筛选出MCLA-158药物的,正是由癌症患者为来源提取培养的类器官!
类器官药筛模型原理
那么类器官是如何进行筛药的?
据专家科普,肿瘤类器官能够在体外高度模拟病人原位肿瘤,这就可以在短时间内高效开展药敏检测,模拟患者对药物的反应。
这相当于在药物进入人体前,可以先在与人体内相似的类器官上进行提前试药,以找到对该患者的最佳治疗方案。
因此类器官被形象地称为患者的 “替身”。
为什么不继续使用现有的2D细胞模型或PDX药筛模型呢?
这是由于2D细胞模型虽然可以在体外进行扩增,但是与人体差异较大,且传代后的细胞会丧失肿瘤异质性。
而用人源化小鼠模型(PDX)进行药物的筛选成功率较低,测试周期也较长(通常需要6到8个月才能出结果),且不具备高通量使用的优势。
肿瘤类器官作为新型药筛模型具有速度快、通量高、临床相关性强的特点。
2018年《Science》杂志报道了首个肠癌类器官药敏临床疗效观察试验,并获得了88%的阳性预测值和100%的阴性预测值的结果,展现了极强的临床相关性。
肿瘤类器官药筛检测流程
肿瘤类器官进行药筛的流程,大致包括类器官的构建、评估、药敏检测三大方面。
1.类器官的构建
类器官构建的样本来源通常为肿瘤组织或者胸腹水等恶性积液。
样本经消化或离心、过滤后分离出肿瘤细胞,然后选择合适的生物材料或者基质胶作为3D培养的细胞外基质,通过模拟肿瘤细胞基质环境进行培养,最后形成体外类器官模型。
类器官培养特有的重要试剂包括消化液、培养基、基质胶等,这些试剂在不同的实验室及培养不同的肿瘤类器官之间的差异较大。
培养过程中添加的生长因子组合需要进行仔细考量,否则失之毫厘,谬以千里。
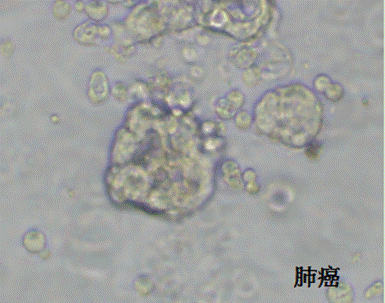
显微镜下的肺癌器官
2.类器官的评估
评估的主要目的是确定类器官和原肿瘤的一致性,运用组织病理学染色和基因测序的方法对培养的类器官与原代肿瘤标本进行对比,显示构建的类器官依然保留着原肿瘤的特性。
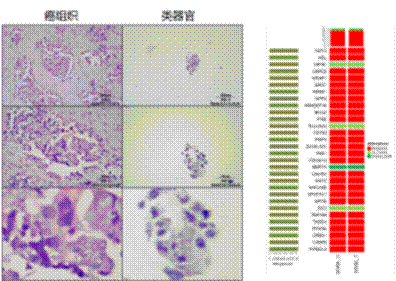
组织病理学染色(左)和基因测序(右)
3.类器官的药筛检测:
类器官目前可筛选的药物种类包括化疗药、小分子靶向药、抗体药物等。通过检测药物的IC50和细胞抑制率,来预测对肿瘤抑制效果最好的药物或药物组合。
肿瘤类器官或成为新型药物研发的重要突破
现如今筛药技术已经趋向于成熟,各种方式的筛药层出不穷,但都有各自的缺陷。
如被广泛用作临床的肿瘤细胞模型和动物模型,在进行筛药过程中,肿瘤细胞模型无法保留原肿瘤的遗传特性和肿瘤微环境,且对药物的耐受性较低,容易出现凋亡。
而动物模型则需要更长的培养周期,更多的培养支出,还会产生伦理风险。
在这种状况下,肿瘤类器官则不存在局限性和伦理考虑。
相较于动物模型,肿瘤类器官有更少的培养周期、减少培养支出,更多的浓度梯度、生理相关度更高。且类器官技术避开了肿瘤细胞模型和动物模型的一些弊端,对药物敏感性检测与配对患者的异质性也更高。
通俗来讲,就是类器官集合了肿瘤细胞模型和动物模型的优点,规避了它们的缺点,使用起来更有效率。
如今,类器官筛药已经开始逐步应用于临床,成为再生领域的一项重大突破,其筛出的药物能够成为临床候选,被官方认可。
我们可以期待,在不久的将来它或可彻底走向成熟,成为临床医学研究和治疗的主流,为新药研发、精准治疗、再生医学等领域带来更加广阔的发展和未来!
咨询热线:
公司地址:辽宁省沈阳市浑南区数字经济产业园F12号
 扫一扫关注官网公众号
扫一扫关注官网公众号
剑兰生物医学科技(辽宁)有限公司 © 1997-2025 辽ICP备2023005865号-1 白帽优化网提供剑兰生物集团官网建站授权技术支持 友情链接: 乐成高科产业集团
剑兰生物医学科技(辽宁)有限公司网站图版文字视频这类版权声明:无法鉴别所上传图片文字视频的知识版权,如果涉猎侵犯版权或违法内容,请及时通知联系我们,官方将在第一时间及时删除!